ตอนที่ 5: แบบจำลองอะตอมของ Bohr: วงโคจรที่เป็นเหมือนขั้นบันได

1. 🎯 ตอนที่ 5: แบบจำลองอะตอมของ Bohr: วงโคจรที่เป็นเหมือนขั้นบันได
2. 📖 เปิดฉาก (The Hook)
สวัสดีครับนักเดินทางแห่งจักรวาลควอนตัม! กลับมาพบกันอีกครั้งที่ร้านกาแฟร้านเดิม ในซีรีส์ ท่องโลกควอนตัม ฉบับคนเกลียดเลขก็อ่านสนุก ครับ
คุณเคยมองดูเก้าอี้ที่คุณนั่ง หรือโต๊ะที่คุณวางแก้วกาแฟ แล้วสงสัยไหมครับว่า “ทำไมมันถึงแข็งแรงและคงรูปอยู่ได้?” คำถามนี้ดูเหมือนจะกำปั้นทุบดิน แต่เชื่อไหมครับว่าในช่วงต้นศตวรรษที่ 20 มันคือฝันร้ายที่ทำให้นักฟิสิกส์ถึงกับนอนไม่หลับ!
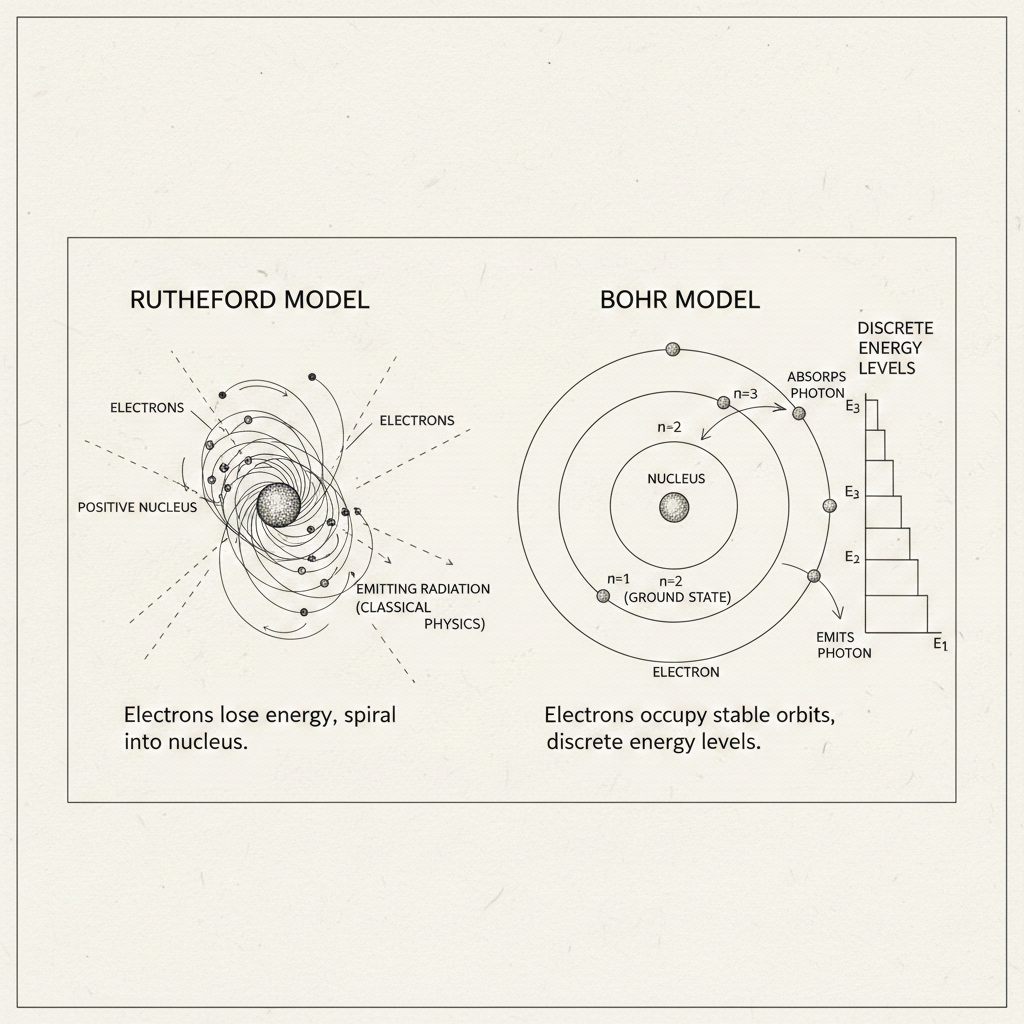
ย้อนกลับไปในปี 1911 เออร์เนสต์ รัทเธอร์ฟอร์ด (Ernest Rutherford) ชายร่างใหญ่ผู้ค้นพบว่าอะตอมไม่ได้เป็นก้อนแป้งที่มีลูกเกดฝังอยู่ (Plum-pudding model) แต่เขาเสนอ แบบจำลองระบบสุริยะ (Planetary Model) ที่บอกว่า อะตอมประกอบด้วยนิวเคลียส (Nucleus) ที่มีประจุบวกอัดแน่นอยู่ตรงกลาง และมีอิเล็กตรอน (Electron) ตัวจิ๋ววิ่งวนรอบๆ เหมือนดาวเคราะห์โคจรรอบดวงอาทิตย์
ฟังดูเมกเซนส์ใช่ไหมครับ? แต่ปัญหามันมีอยู่ว่า… ตามกฎแม่เหล็กไฟฟ้าคลาสสิกของแมกซ์เวลล์ (Maxwell’s equations) เมื่อประจุไฟฟ้าอย่างอิเล็กตรอนวิ่งโคจรเป็นวงกลม มันจะต้องสูญเสียพลังงานและแผ่รังสีออกมาตลอดเวลา พลังงานที่ลดลงจะทำให้อิเล็กตรอนวิ่งช้าลง แล้วค่อยๆ หมุนควงสว่านตกลงไปชนกับนิวเคลียส
นักฟิสิกส์คำนวณออกมาแล้วพบว่า อะตอมแบบรัทเธอร์ฟอร์ดจะพังทลายลงภายในเวลาเพียง $1 \times 10^{-12}$ วินาที (หนึ่งในล้านล้านวินาที)! ถ้ากฎคลาสสิกเป็นจริง ตัวคุณ โต๊ะ เก้าอี้ และจักรวาลนี้ไม่ควรมีอยู่จริงครับ! โชคดีที่ชายหนุ่มชาวเดนมาร์กนามว่า นีลส์ บอร์ (Niels Bohr) ก้าวเข้ามาช่วยกู้โลก (และกู้อะตอม) ไว้ได้ทันเวลา!
3. 🧠 แก่นวิชา (The Mind-Blowing Concepts)
นีลส์ บอร์ เป็นนักทฤษฎีหนุ่มที่เดินทางไปทำงานกับรัทเธอร์ฟอร์ดที่แมนเชสเตอร์ เขาเห็นปัญหาของอะตอมแบบคลาสสิกที่กำลังจะพังทลายลง บอร์จึงเสนอไอเดียสุดบ้าบิ่นในปี 1913 โดยหยิบเอาแนวคิด “ควอนตัม” (Quantum) หรือพลังงานที่เป็นก้อนๆ ของพลังค์และไอน์สไตน์ มาใช้กับโครงสร้างอะตอมซะเลย!
บอร์ได้ตั้งสมมติฐานใหม่ที่ฉีกทุกกฎของฟิสิกส์คลาสสิก เรียกว่า Bohr’s Atomic Model:
- วงโคจรต้องห้าม: อิเล็กตรอนไม่ได้วิ่งรอบนิวเคลียสอย่างอิสระตรงไหนก็ได้ แต่มันถูกบังคับให้อยู่ใน “ระดับพลังงาน” (Energy Levels) หรือวงโคจรพิเศษที่กำหนดไว้เท่านั้น
- กฎขั้นบันได (The Staircase Analogy): ลองจินตนาการถึง “ขั้นบันได” ครับ อิเล็กตรอนเปรียบเสมือนสุนัขที่กำลังหาที่นอน มันสามารถนอนบนบันไดขั้นที่ 1 (ชั้นในสุด) หรือขั้นที่ 2 หรือขั้นที่ 3 ได้… แต่มัน “ไม่สามารถ” ลอยตัวนอนอยู่กลางอากาศระหว่างขั้นที่ 1 กับ 2 ได้!
- วงโคจรอมตะ: ตราบใดที่อิเล็กตรอนยังวิ่งอยู่ในวงโคจรพิเศษเหล่านี้ (Stationary states) มันจะ “ไม่สูญเสียพลังงาน” และไม่แผ่รังสีใดๆ ออกมาเลย (หักล้างกฎของแมกซ์เวลล์ดื้อๆ เลยครับ!)
การมีอยู่ของ “บันไดขั้นล่างสุด” หรือที่เรียกว่า Ground State (สถานะพื้น) นี่แหละครับ คือคำตอบว่าทำไมอิเล็กตรอนถึงไม่ตกลงไปชนนิวเคลียส… ก็เพราะมันไม่มีบันไดขั้นที่ต่ำกว่านี้ให้มันตกลงไปอีกแล้ว! อะตอมจึงเสถียร และตัวคุณก็เลยไม่สลายกลายเป็นฝุ่นผงครับ!
4. 🔬 ร่ายมนต์สมการและการทดลอง (The Science & Experiments)
แล้วการที่มันจะเปลี่ยนวงโคจรล่ะ ทำยังไง? นี่คือที่มาของคำศัพท์ฮิตติดปากอย่าง “Quantum Leap” (การก้าวกระโดดทางควอนตัม) ครับ!
เมื่ออิเล็กตรอนได้รับพลังงานจากภายนอก (เช่น ถูกแสงส่อง หรือโดนความร้อน) มันจะดูดซับ “โฟตอน” (Photon) เข้าไป แต่มีข้อแม้ว่า พลังงานของโฟตอนนั้นต้อง “พอดีเป๊ะ” กับความสูงของขั้นบันได! ถ้ารับพลังงานพอดี มันจะกระโดดแว้บ! ขึ้นไปอยู่บันไดขั้นที่สูงกว่า เรียกว่า Excited state (สถานะกระตุ้น)
แต่มันอยู่ชั้นบนได้ไม่นานหรอกครับ มันอยากกลับมาเสถียรที่ชั้นล่าง มันจึงกระโดดกลับลงมา พร้อมกับคายพลังงานส่วนเกินทิ้งไปในรูปของ “แสง” (Photon) ซึ่งพลังงานที่คายออกมาก็คำนวณได้จากสมการอมตะ:
$$ \Delta E = hf $$
- $\Delta E$ คือ ความแตกต่างของพลังงานระหว่างวงโคจรสองวง (ชั้นบน ลบ ชั้นล่าง)
- $h$ คือ ค่าคงตัวของพลังค์ (Planck’s constant)
- $f$ (หรือ $\nu$) คือ ความถี่ของแสงที่ปล่อยออกมา
สมการนี้ของบอร์ อธิบายปรากฏการณ์ที่เรียกว่า Atomic Line Spectra (สเปกตรัมเส้นสว่าง) ได้อย่างสมบูรณ์แบบ มันไขปริศนาได้ว่า ทำไมก๊าซไฮโดรเจนถึงเปล่งแสงออกมาเป็นเส้นสีแดง สีฟ้า สีม่วง ที่มีความยาวคลื่นเฉพาะตัวตายตัวเท่านั้น (รู้จักกันในชื่อ Balmer series) ก็เพราะแต่ละเส้นสี เกิดจากระยะห่างของขั้นบันไดแต่ละขั้นในอะตอมนั่นเองครับ!
5. 🛡️ เรื่องแปลกแต่จริง (Weird Quantum Facts)
แนวคิดแบบจำลองของบอร์ พาเราไปเจอเรื่องประหลาดที่ขัดกับสามัญสำนึกอีกเพียบเลยครับ:
- การวาร์ปแบบไม่มีการเดินทาง (Teleportation): เวลาที่อิเล็กตรอนกระโดดจากขั้นที่ 1 ไปขั้นที่ 2 (Quantum Leap) มันไม่ได้ค่อยๆ ลอยขึ้นไปแบบลิฟต์หรือจรวดนะครับ แต่มันหายตัววับจากชั้นที่ 1 แล้วไปโผล่ที่ชั้นที่ 2 ทันที! มันไม่ได้ใช้เวลาเดินทางผ่านพื้นที่ว่างตรงกลางเลย นี่มันวิชาเคลื่อนย้ายพริบตาชัดๆ!
- ที่มาของคำว่า Quantum Leap: คนทั่วไปชอบเอาคำว่า “Quantum Leap” ไปใช้เปรียบเปรยถึง “การก้าวกระโดดที่ยิ่งใหญ่และกว้างไกล” แต่ในทางฟิสิกส์แล้ว การก้าวกระโดดระดับควอนตัม คือการเปลี่ยนแปลงที่ “เล็กที่สุด” เท่าที่จะเป็นไปได้ในจักรวาลต่างหากครับ!
- นักคำนวณผู้ดื้อรั้น: บอร์ถึงกับเอาสูตรของตัวเองไปหาขนาดของอะตอมไฮโดรเจนในสถานะพื้น และได้ตัวเลขออกมาที่ $0.529 \times 10^{-10}$ เมตร ซึ่งปัจจุบันเราให้เกียรติเรียกตัวเลขนี้ว่า Bohr radius (รัศมีของบอร์)
6. 🏁 บทสรุป (To be continued…)
แบบจำลองของนีลส์ บอร์ ถือเป็นการกอบกู้วิกฤตฟิสิกส์ครั้งยิ่งใหญ่ เขาอธิบายโครงสร้างอะตอมไฮโดรเจนได้อย่างสวยงาม และเป็นจุดเริ่มต้นของเคมีสมัยใหม่ที่ทำให้เราเข้าใจการเรียงตัวของอิเล็กตรอนในตารางธาตุ
แต่… ความสุขมักอยู่ไม่นานครับ เมื่อนักวิทยาศาสตร์พยายามเอาแบบจำลองของบอร์ ไปคำนวณกับอะตอมที่ซับซ้อนขึ้นอย่างฮีเลียม (ที่มี 2 อิเล็กตรอน) สมการของบอร์กลับพังไม่เป็นท่า! การมองว่าอิเล็กตรอนเป็นแค่ “เม็ดลูกกลมๆ จิ๋วๆ” ที่วิ่งบนรางรถไฟวงกลม มันเริ่มไปต่อไม่ได้แล้ว
เกิดอะไรขึ้นกับอิเล็กตรอน? หรือว่าแท้จริงแล้วมันไม่ใช่ “อนุภาค” อย่างที่เราคิดมาตลอด? เตรียมพบกับชายหนุ่มผู้มีสายเลือดขุนนางฝรั่งเศส หลุยส์ เดอ บรอยล์ (Louis de Broglie) ที่จะมาพลิกวงการอีกครั้ง ด้วยการเสนอว่า “ถ้าแสงเป็นอนุภาคได้… สสารก็ต้องเป็นคลื่นได้เหมือนกันสิ!” ในตอนหน้าของซีรีส์ครับ ห้ามพลาด!
สนใจพูดคุยแลกเปลี่ยนแนวคิดทางวิทยาศาสตร์ หรือปรึกษาการนำเทคโนโลยีไปใช้พัฒนาองค์กรของคุณ? ทีมงาน WP Solution พร้อมให้บริการออกแบบและติดตั้งระบบไอทีแบบครบวงจร ดูรายละเอียดบริการของเราได้ที่: www.wpsolution2017.com หรือพูดคุยปรึกษาเบื้องต้นได้ที่ Line: wisit.p